研究の背景INTRODUCTION
腫瘍内低酸素領域とは?
細胞の無限増殖やアポトーシスの回避等に代表されるがんの特性は、がん細胞の増殖速度と腫瘍血管の形成速度とのアンバランスを引き起こします。結果として、悪性腫瘍の内部には、十分な酸素が供給されない低酸素領域が生じます(慢性低酸素)[1]。また、腫瘍の増殖に遅れて構築される腫瘍血管は正常組織のそれと比較して脆弱であり、かつ遮断や逆流を繰り返すため、腫瘍血管の近傍にも一過性の低酸素環境が生じることが知られています(急性低酸素)。この様な血流不足はがん細胞の増殖遅延や抗がん剤のデリバリー不足に繋がりますので、低酸素環境にあるがん細胞は一般的な抗がん剤に抵抗性を示します[2]。また、エックス線やガンマ線の殺細胞効果は酸素の存在に強く依存することから、低酸素環境にあるがん細胞は放射線治療にも抵抗性を示すことが報告されています[3]。さらに、低酸素環境にあるがん細胞は運動・遊走能を亢進することによって劣悪な環境からの回避を図り、これががんの転移・浸潤能の亢進につながると言われています[4,5]。この様に、およそ“低酸素”のまわりには、がんの克服を妨げる様々な負の因子が渦巻いていると言えます。がん研究において低酸素バイオロジーが注目されてきたのは、極めて自然な流れであると言えるでしょう。
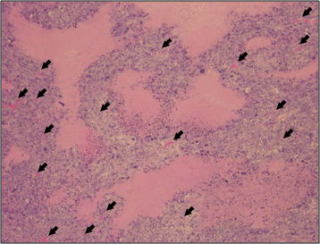
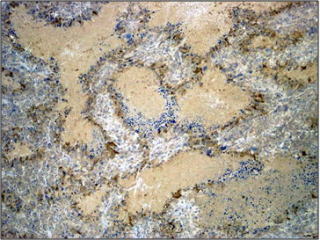
H&E染色(左)、及び低酸素マーカー(ピモニダゾール)で染色(右)した悪性腫瘍の切片。左図の矢印で示される腫瘍血管の周りには、十分な酸素が供給されるがん細胞が存在します。腫瘍血管から70-100ミクロン程度離れた領域には壊死したがん細胞が存在します。両者の境界に存在する低酸素領域が、低酸素マーカー(右図のブラウン)によって見てとれます。
- Vaupel P et al. Cancer Res 49:6449-6465. 1989
- Teicher BA. Cancer Metastasis Rev 13: 139-168. 1994.
- Thomlinson RH, Gray LH. Br J Cancer 9: 539-549. 1955.
- Pennacchietti S et al. Cancer Cell. 3: 347-361. 2003.
- Rofstad EK. Int J Radiat Biol. 76: 589-605. 2000.
細胞の低酸素適応応答におけるHIF-1の機能
近年の分子細胞生物学の進展により、がん細胞がHypoxia-inducible Factor 1(HIF-1)という転写因子を活性化して、低酸素環境への適応を図ることが明らかになってきました。 HIF-1はalphaサブユニット(HIF-1α)とbetaサブユニット(HIF-1β)からなるヘテロダイマーで、その活性は主にHIF-1αタンパク質の修飾と安定性に依存していることが明らかになってきました。 すなわち、酸素存在下にある細胞内でHIF-1αはプロテアソーム系によって速やかに分解されるため、転写を活性化することができなくなります。 一方、低酸素環境にある細胞内でHIF-1αは安定化し、HIF-1βと協調して特異的エンハンサー配列hypoxia-response element( HRE)に結合します。 そしてvascular endothelial cell growth factor (VEGF)をはじめとする遺伝子群の発現を誘導して、自身に新たな血管系を呼び込み(いわゆる血管新生)、酸素環境の改善を図ります。 また、HIF-1はグルコーストランスポーターやヘキソキナーゼに代表される解糖系関連遺伝子の発現を誘導するとともに、ミトコンドリアによる酸化的リン酸化を抑制することによって、低酸素環境下での効率良いATPの生成を図ります。 その他、低酸素環境からのがん細胞の回避(転移・浸潤)や、低酸素環境で発生する活性酸素種の軽減といった重要な生命活動が、HIF-1の下流遺伝子に依存していることが分かってきました。
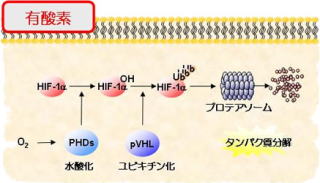
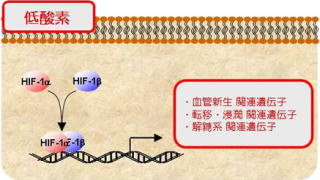
有酸素環境下でHIF-1αタンパク質はプロリン水酸化酵素(PHDs)によって水酸化され、さらにvon Hippel Lindau (VHL)によってユビキチン化されます。一連の修飾が引き金となって、プロテアソームによって速やかに分解されます。一方、低酸素環境下でHIF-1αタンパク質は安定化し、HIF-1βと結合して転写因子HIF-1を形成して血管新生、解糖系、転移、浸潤等に関わる様々な遺伝子発現を誘導します。
LINKS

※その他のリンクはこちら
LAB INFORMATION
京都大学大学院
生命科学研究科
がん細胞生物学分野
〒606-8501
京都市左京区吉田近衛町
TEL: 075-753-7560
FAX: 075-753-7564
